Здесь теория. Вы также можете перейти к выбору приборов из этого раздела.
 Спектроскопия
Спектроскопия 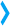
Спектроскопия — это изучение взаимодействия между веществом и электромагнитным излучением в зависимости от длины волны или частоты излучения. Исторически спектроскопия возникла как изучение зависимости поглощения газовой фазой вещества видимого света, рассеянного призмой, от длины волны.
Спектроскопия, в первую очередь в электромагнитном спектре, является фундаментальным инструментом исследования в области физики, химии и астрономии, позволяя изучать состав, физическую структуру и электронную структуру материи в атомном, молекулярном и макромасштабе, а также на астрономических расстояниях. Важные приложения биомедицинской спектроскопии возникают в области анализа тканей и медицинской визуализации.
Спектроскопия — это отрасль науки, изучающая спектры электромагнитного излучения в зависимости от длины волны или частоты, измеряемые спектрографическим оборудованием и другими методами для получения информации о структуре и свойствах вещества. Устройства для спектральных измерений называют спектрометрами, спектрофотометрами, спектрографами или спектральными анализаторами. Большинство спектральных анализов в лаборатории начинается с образца, подлежащего анализу, затем выбирается источник света из любого желаемого диапазона светового спектра, затем свет проходит через образец на дисперсионную решетку (прибор с дифракционной решеткой) и улавливается фотодиодом. Для астрономических целей телескоп должен быть оснащен устройством для дисперсии света. Существуют различные варианты этой базовой установки, которые могут быть использованы.
Спектроскопия как наука началась с того, что Исаак Ньютон расщепил свет с помощью призмы и была названа оптикой. Таким образом, первоначально она была изучением видимого света, который мы называем цветом, но позже под влиянием исследований Джеймса Клерка Максвелла стала включать в себя весь электромагнитный спектр. Хотя в спектроскопии задействован цвет, он не приравнивается к цвету элементов или объектов, которые включают в себя поглощение и отражение определенных электромагнитных волн, чтобы придать объектам ощущение цвета для наших глаз. Скорее, спектроскопия подразумевает расщепление света призмой, дифракционной решеткой или аналогичным инструментом, чтобы получить определенный дискретный рисунок линий, называемый "спектром", уникальный для каждого типа элемента. Большинство элементов сначала помещают в газообразную фазу, чтобы можно было исследовать спектры, хотя сегодня можно использовать и другие методы на различных фазах. Каждый элемент, дифрагированный прибором, напоминающим призму, показывает либо спектр поглощения, либо спектр испускания в зависимости от того, охлаждается или нагревается элемент.
До недавнего времени вся спектроскопия включала в себя изучение спектров линий, и большинство спектроскопии до сих пор изучает их. Колебательная спектроскопия — это та ветвь спектроскопии, которая изучает спектры. Однако последние достижения в спектроскопии позволяют иногда обойтись без метода дисперсии. В биохимической спектроскопии информация о биологической ткани может быть собрана с помощью методов поглощения и рассеяния света. Спектроскопия рассеяния света — это разновидность спектроскопии отражения, которая определяет структуру тканей путем изучения упругого рассеяния. В этом случае именно ткань выступает в качестве дифракционного или дисперсионного механизма.
Спектроскопические исследования были центральными для развития квантовой механики, потому что первые полезные атомные модели описывали спектры водорода, которые включают модель Бора, уравнение Шредингера и матричную механику, которые все могут производить спектральные линии водорода, таким образом, обеспечивая основу для дискретных квантовых переходов, чтобы соответствовать дискретному спектру водорода. Кроме того, Макс Планк объяснил излучение черного тела с помощью спектроскопии, поскольку он сравнивал длину волны света с помощью фотометра с температурой черного тела. Спектроскопия используется в физической и аналитической химии, поскольку атомы и молекулы имеют уникальные спектры. В результате эти спектры могут быть использованы для обнаружения, идентификации и количественной оценки информации об атомах и молекулах. Спектроскопия также используется в астрономии и дистанционном зондировании Земли. Большинство исследовательских телескопов оснащены спектрографами. Измеренные спектры используются для определения химического состава и физических свойств астрономических объектов (таких как их температура, плотность элементов в звезде, скорость, черные дыры и многое другое). Важное применение спектроскопия находит в биохимии. Молекулярные образцы могут быть проанализированы для идентификации видов и содержания энергии.
Центральная теория спектроскопии заключается в том, что свет состоит из различных длин волн и что каждая длина волны соответствует различной частоте. Важность спектроскопии заключается в том, что каждый элемент в периодической таблице имеет уникальный световой спектр, описываемый частотами света, который он излучает или поглощает, последовательно появляясь в одной и той же части электромагнитного спектра при дифракции света. Это открыло целую область для изучения всего, что содержит атомы, то есть всей материи. Спектроскопия — это ключ к пониманию атомных свойств всей материи. Спектроскопия как таковая открыла множество новых, еще не открытых областей науки. Идея о том, что каждый атомный элемент имеет свою уникальную спектральную подпись, позволила использовать спектроскопию в широком спектре областей, каждая из которых преследует конкретную цель, достигаемую с помощью различных спектроскопических процедур. Эти уникальные спектральные линии для каждого элемента настолько важны для многих отраслей науки, что правительство ведет общедоступную базу данных атомных спектров, которая постоянно пополняется более точными измерениями на сайте NIST.
Расширение области спектроскопии связано с тем, что для анализа образца может быть использована любая часть электромагнитного спектра — от инфракрасного до ультрафиолетового, что сообщает ученым различные свойства одного и того же образца. Например, в химическом анализе наиболее распространенными видами спектроскопии являются атомная спектроскопия, инфракрасная спектроскопия, ультрафиолетовая и видимая спектроскопия, спектроскопия Рамана и ядерный магнитный резонанс. В ядерном магнитном резонансе теория заключается в том, что частота аналогична резонансу и соответствующей ему резонансной частоте. Резонансы по частоте были впервые охарактеризованы в механических системах, таких как маятники, которые имеют частоту движения, отмеченную знаменитым Галилеем.
Спектроскопия является достаточно широкой областью, в которой существует множество поддисциплин, каждая из которых имеет многочисленные реализации конкретных спектроскопических методов. Различные реализации и техники могут быть классифицированы несколькими способами.
Виды спектроскопии различаются по типу излучаемой энергии, участвующей во взаимодействии. Во многих приложениях спектр определяется путем измерения изменений в интенсивности или частоте этой энергии. К изучаемым типам излучаемой энергии относятся:
Электромагнитное излучение было первым источником энергии, используемым для спектроскопических исследований. Методы, использующие электромагнитное излучение, обычно классифицируются по области длин волн спектра и включают микроволновую, терагерцовую, инфракрасную, ближнюю инфракрасную, ультрафиолетово-видимую, рентгеновскую и гамма-спектроскопию.
Частицы, благодаря своим волнам де Бройля, также могут быть источником лучистой энергии. Обычно используется электронная и нейтронная спектроскопия. Для частицы ее кинетическая энергия определяет длину волны.
В акустической спектроскопии используются излучаемые волны давления.
Динамический механический анализ может быть использован для придания твердым материалам энергии излучения, подобной акустическим волнам.
Типы спектроскопии также можно различать по характеру взаимодействия между энергией и материалом. К таким взаимодействиям относятся:
Абсорбционная спектроскопия: Поглощение происходит, когда энергия от источника излучения поглощается материалом. Поглощение часто определяется путем измерения доли энергии, проходящей через материал, при этом поглощение уменьшает проходящую часть.
Эмиссионная спектроскопия: Эмиссия указывает на то, что излучаемая энергия высвобождается материалом. Спектр черного тела материала — это спектр спонтанного излучения, определяемый его температурой. Эта характеристика может быть измерена в инфракрасном диапазоне такими приборами, как атмосферный интерферометр излучения. Эмиссия также может быть вызвана другими источниками энергии, такими как пламя, искры, электрическая дуга или электромагнитное излучение в случае флуоресценции.
Упругое рассеяние и спектроскопия отражения определяют, как падающее излучение отражается или рассеивается материалом. Кристаллография использует рассеяние высокоэнергетического излучения, такого как рентгеновские лучи и электроны, для изучения расположения атомов в белках и твердых кристаллах.
Импедансная спектроскопия: Импеданс — это способность среды препятствовать или замедлять передачу энергии. Для оптических приложений это характеризуется показателем преломления.
Явления неупругого рассеяния подразумевают обмен энергией между излучением и веществом, который смещает длину волны рассеянного излучения. К ним относятся рамановское и комптоновское рассеяние.
Когерентная или резонансная спектроскопия — это методы, в которых энергия излучения связывает два квантовых состояния материала в когерентном взаимодействии, которое поддерживается излучающим полем. Когерентность может быть нарушена другими взаимодействиями, такими как столкновения частиц и перенос энергии, поэтому для ее поддержания часто требуется излучение высокой интенсивности. Спектроскопия ядерного магнитного резонанса (ЯМР) является широко используемым резонансным методом, также возможна сверхбыстрая лазерная спектроскопия в инфракрасной и видимой областях спектра.
Ядерная спектроскопия — это методы, использующие свойства конкретных ядер для исследования локальной структуры в веществе, главным образом в конденсированном веществе, молекулах в жидкостях или замороженных жидкостях и биомолекулах.
Спектроскопические исследования построены таким образом, что лучистая энергия взаимодействует с определенными типами материи.
Атомная спектроскопия была первым разработанным применением спектроскопии. Атомная абсорбционная спектроскопия и атомная эмиссионная спектроскопия используют видимый и ультрафиолетовый свет. Эти поглощения и испускания, часто называемые атомными спектральными линиями, обусловлены электронными переходами электронов внешней оболочки, когда они поднимаются и опускаются с одной электронной орбиты на другую. Атомы также имеют различные рентгеновские спектры, которые обусловлены возбуждением электронов внутренней оболочки в возбужденные состояния.
Атомы различных элементов имеют различные спектры, поэтому атомная спектроскопия позволяет идентифицировать и количественно определять элементный состав образца. После изобретения спектроскопа Роберт Бунзен и Густав Кирхгоф открыли новые элементы, наблюдая их эмиссионные спектры. Атомные линии поглощения наблюдаются в солнечном спектре и называются линиями Фраунгофера в честь их первооткрывателя. Всестороннее объяснение спектра водорода стало ранним успехом квантовой механики и объяснило наблюдаемый в спектре водорода сдвиг Лэмба, что в дальнейшем привело к развитию квантовой электродинамики.
Современные реализации атомной спектроскопии для изучения видимых и ультрафиолетовых переходов включают эмиссионную спектроскопию пламени, атомную эмиссионную спектроскопию индуктивно связанной плазмы, спектроскопию тлеющего разряда, спектроскопию плазмы, индуцированной микроволнами, и эмиссионную спектроскопию искры или дуги. Методы изучения рентгеновских спектров включают рентгеновскую спектроскопию и рентгеновскую флуоресценцию.
Объединение атомов в молекулы приводит к созданию уникальных типов энергетических состояний и, следовательно, уникальных спектров переходов между этими состояниями. Молекулярные спектры могут быть получены благодаря электронным спиновым состояниям (электронный парамагнитный резонанс), молекулярным вращениям, молекулярным вибрациям и электронным состояниям. Вращения являются коллективными движениями атомных ядер и обычно приводят к спектрам в микроволновой и миллиметроволновой областях спектра. Вращательная спектроскопия и микроволновая спектроскопия являются синонимами. Колебания — это относительные движения атомных ядер, которые изучаются с помощью инфракрасной и рамановской спектроскопии. Электронные возбуждения изучаются с помощью видимой и ультрафиолетовой спектроскопии, а также флуоресцентной спектроскопии.
Исследования в области молекулярной спектроскопии привели к созданию первого мазера и способствовали последующему развитию лазера.
Объединение атомов или молекул в кристаллы или другие протяженные формы приводит к созданию дополнительных энергетических состояний. Эти состояния многочисленны и поэтому имеют высокую плотность состояний. Эта высокая плотность часто делает спектры слабее и менее отчетливыми, т.е. более широкими. Например, излучение черного тела обусловлено тепловыми движениями атомов и молекул внутри материала. Акустические и механические отклики также обусловлены коллективными движениями. Чистые кристаллы, однако, могут иметь отчетливые спектральные переходы, и расположение кристаллов также влияет на наблюдаемые молекулярные спектры. Регулярная решетчатая структура кристаллов также рассеивает рентгеновские лучи, электроны и нейтроны, что позволяет проводить кристаллографические исследования.
Ядра также имеют различные энергетические состояния, которые широко разделены и приводят к спектрам гамма-излучения. Различные состояния ядерного спина могут разделяться по энергии магнитным полем, что позволяет проводить спектроскопию ядерного магнитного резонанса.
Существует несколько областей применения спектроскопии в медицине, физике, химии и астрономии. Используя свойства поглощения, а в астрономии — испускания, спектроскопия может быть использована для определения определенных состояний природы. Использование спектроскопии в столь разных областях и для столь разных применений привело к появлению специальных научных подполей. К таким примерам относятся: